创新药企BD交易火热,VC/PE赋能海外拓展
AI导读:
2025年创新药企license out交易持续火热,VC/PE机构助力创新药企对接海外需求、拓展海外市场。恒瑞医药、和铂医药等多家上市药企宣布与海外药企达成合作,并获得高额里程碑付款。海外授权给药企带来可观资金流,但出海谈判周期长、不确定性高,仍需VC/PE支持。
日前,恒瑞医药与美国医药巨头默沙东(MSD)达成协议,将其脂蛋白(a)[Lp(a)]口服小分子项目(先导化合物名为HRS-5346)有偿许可给默沙东,默沙东将获得该项目在大中华区以外的全球独家开发、生产和商业化权利。这一交易再次点燃了2025年创新药企license out(许可输出)市场的热情。
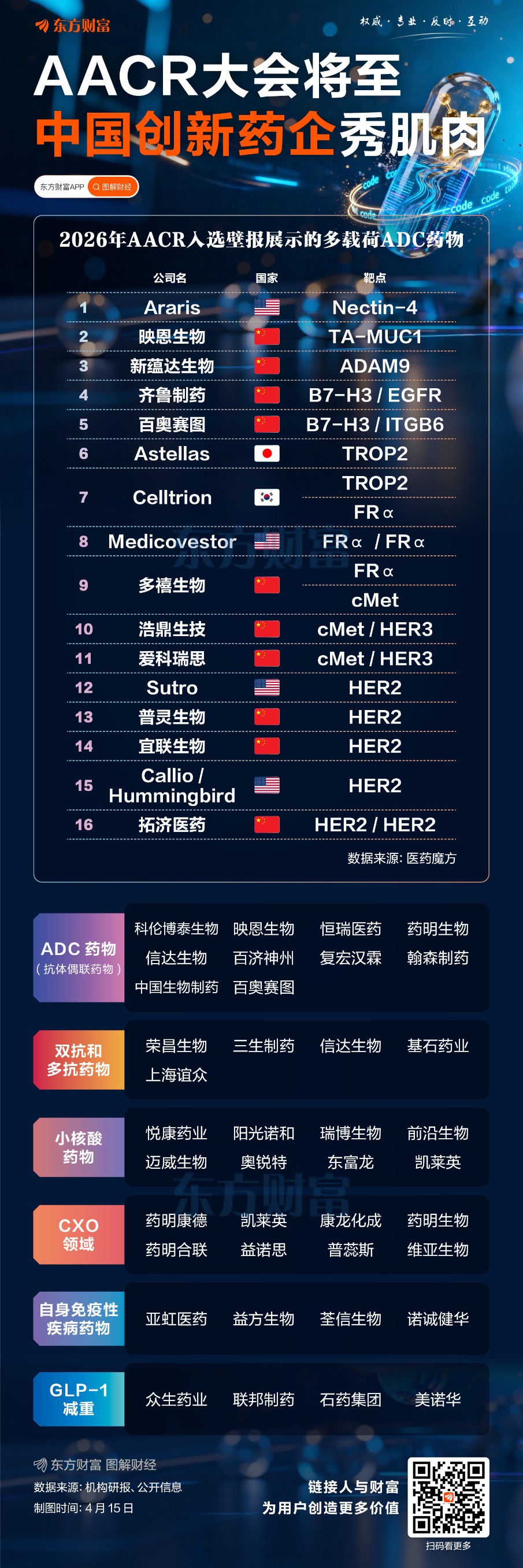
据统计,仅开年前两个月,中国创新药BD(商务拓展)项目已达16项,合作领域从肿瘤拓展至自免等新兴方向。手握资金和资源的创新药VC/PE(风险投资和私募股权投资)机构成为这场交易热潮的“赋能者”,助力创新药企对接海外需求、拓展海外市场。
在这场创新药BD交易盛宴中,恒瑞医药、和铂医药、信达生物等多家上市药企纷纷宣布与海外药企达成合作,并获得高额的里程碑付款。VC/PE机构不仅积极参与其中,还通过其资源和网络,为创新药企提供更多的市场机会和资金支持。
LongRiver江远投资合伙人李佳安观察到,今年的创新药BD商业模式更加明确,增速可观。他所在的企业安锐生物去年已达成两笔授权出海交易,金额超过15亿美元。此外,据DealForma数据显示,2024年全球31%的跨国药企引进的创新药候选分子来自中国。
在药企BD背后,VC/PE机构发挥着重要的作用。它们不仅为创新药企提供资金支持,还帮助其进行BD业务,对接海外需求。创东方投资合伙人卢刚表示,海外BD或将是企业实现输血、投资机构实现退出的路径之一。数据显示,2023年药企BD交易金额已超过IPO融资金额。
在买家方面,阿斯利康、诺华、强生等跨国药企巨头以及中国本土大药企成为主力。这些买家通过BD交易获取创新药管线,补充自身产品线,提升竞争力。同时,海外基金也开始关注中国创新药企,寻求First-in-class(首创新药)的机会。
然而,药企出海并非一帆风顺。据统计,2019年至2024年期间,真正实现大额BD交易(合同金额大于1亿美元)的创新药案例数仅占同期实现融资案例总数的约6%。实现大额BD交易需要创新药企具备临床数据、差异化优势等因素。
海外授权给药企带来的短期资金流确实可观。和誉医药、和铂医药等公司通过BD交易实现盈利。但药企BD并非仅仅为了补充现金流,更是为了加速国际化进程、分摊研发风险。
对于VC/PE机构而言,虽然药企BD难以全面解决其退出难的问题,但相比IPO对创新药企管线所在的阶段要求更为宽松,因此一定程度上也是实现投资退出的有效补充。
中国创新药企正通过一个个BD交易案频频亮相国际市场,刷新全球对中国药企的认知。海外BD的合同总金额通常超过企业现有估值/市值的数十倍,显示出中国创新药企的崛起和竞争力。
虽然药企BD势头迅猛,但海外授权占融资案例数量占比仍然较小,且项目大多偏后期。因此,创新药企的融资依然非常需要一级市场VC/PE的支持。
(文章来源:证券时报)
郑重声明:以上内容与本站立场无关。本站发布此内容的目的在于传播更多信息,本站对其观点、判断保持中立,不保证该内容(包括但不限于文字、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关内容不对各位读者构成任何投资建议,据此操作,风险自担。股市有风险,投资需谨慎。如对该内容存在异议,或发现违法及不良信息,请发送邮件至yxiu_cn@foxmail.com,我们将安排核实处理。